De behandeling van niet-kleincellige longkanker met EGFR-mutaties is in een stroomversnelling geraakt door de opkomst van gerichte therapieën. Waar voorheen chemotherapie de standaard was, hebben tyrosinekinaseremmers geleid tot aanzienlijke verbeteringen in de overleving.1,2 Toch blijven er klinische uitdagingen bestaan, zoals therapieresistentie, bijwerkingen en de praktische belasting van intraveneuze behandelingen. Tijdens het European Lung Cancer Congress 2025 werden recente onderzoeksresultaten gepresenteerd die op meerdere fronten verbetering beloven: effectievere combinatietherapieën, strategieën ter preventie van bijwerkingen en patiëntvriendelijkere toedieningsvormen. In dit artikel worden de bevindingen uit de MARIPOSA-studie (gericht op effectiviteit en overleving) en de PALOMA-studies (gericht op subcutane versus intraveneuze toediening) besproken.3-6
Niet-kleincellige longkanker (NSCLC) vormt ongeveer 85% van alle longkankers en is wereldwijd een van de belangrijkste doodsoorzaken door kanker.7 Binnen deze groep komen epidermale groeifactorreceptor (EGFR)-mutaties relatief frequent voor, met name bij patiënten van Aziatische afkomst en bij niet-rokers.8,9 Deze mutaties bieden een doelwit voor gerichte therapieën met tyrosinekinaseremmers (TKI’s) die in de afgelopen jaren de standaardeerstelijnsbehandeling zijn geworden voor patiënten met gemetastaseerd EGFR-gemuteerd NSCLC.10 Ondanks deze ontwikkelingen blijft de overleving voor deze patiënten beperkt. De eerste generatie TKI’s resulteerde in een mediane overleving van 31,8 maanden.2 De derde generatie TKI osimertinib resulteerde in een verlenging van de mediane overleving naar 38,6 maanden.2 Toch ontwikkelen veel patiënten uiteindelijk resistentie, vaak als gevolg van MET-amplificatie of secundaire EGFR-mutaties.11 Om deze uitdagingen te adresseren zijn combinaties van behandelingen ontwikkeld die gericht zijn op meerdere oncogene mechanismen tegelijk.
MARIPOSA-studie: significant langere overleving3,4
Tijdens het European Lung Cancer Congress (ELCC) werden data uit de MARIPOSA-studie gedeeld, waarin de combinatie van amivantamab + lazertinib (n = 429) versus osimertinib (n = 429) werd onderzocht als eerstelijnsbehandeling bij patiënten met gemetastaseerd EGFR-gemuteerd NSCLC. Belangrijke eindpunten waren progressievrije overleving (PFS), overall survival (OS), intracraniële progressie (icPFS), en tijd tot symptomatische progressie (TTSP).3,4 De mediane OS voor patiënten die de combinatie amivantamab + lazertinib kregen werd niet bereikt, in tegenstelling tot 36,7 maanden voor patiënten die alleen osimertinib kregen. De hazard ratio (HR) voor sterfte was 0,75 (95%-BI 0,61-0,92; p < 0,005) (figuur 1).3,4 Op basis van een exponentiële distributie-veronderstelling van de OS in beide groepen, wordt verwacht dat de verbetering in mediane OS meer dan 1 jaar zal zijn.3,4
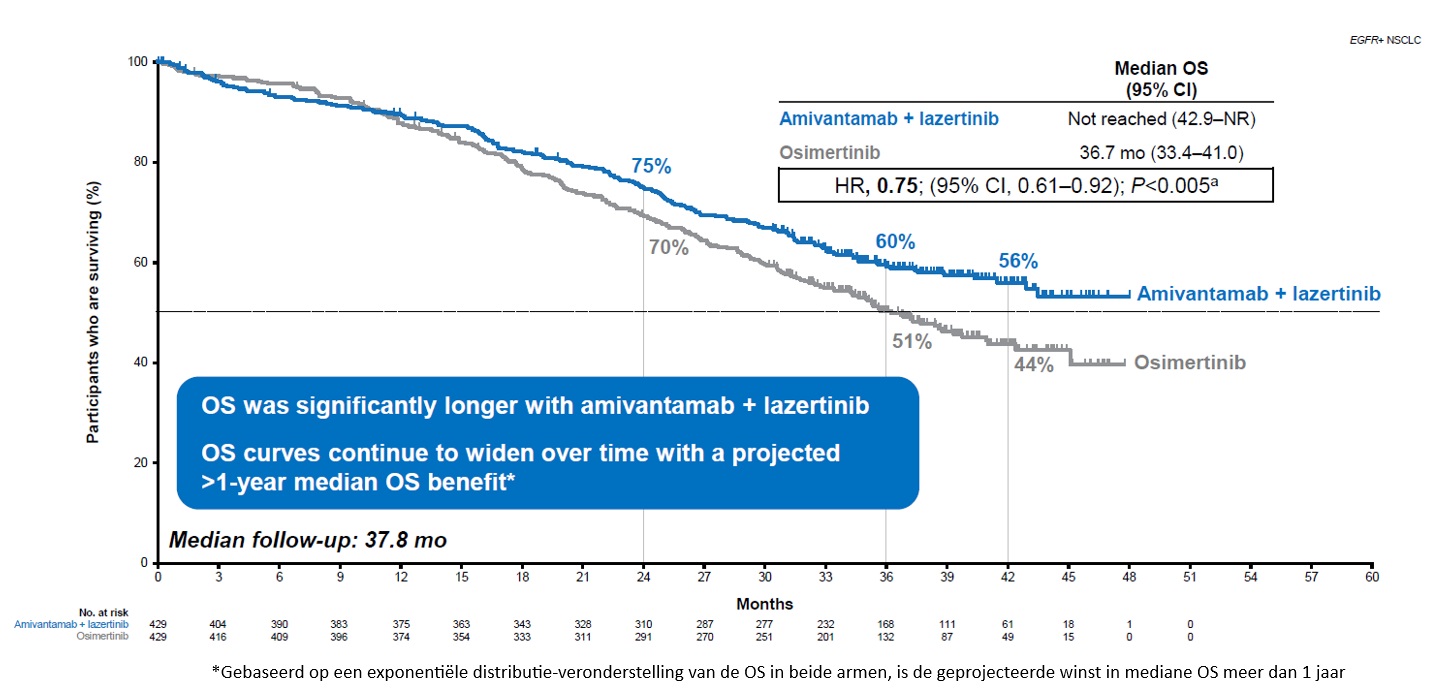
Figuur 1. Overall survival in de MARIPOSA-studie3,4
*Gebaseerd op een exponentiële distributie-veronderstelling van de OS in beide armen, is de geprojecteerde winst in mediane OS meer dan 1 jaar
Het OS-voordeel van amivantamab + lazertinib bleek in nagenoeg alle vooraf gedefinieerde subgroepen consistent, zoals onder meer bij patiënten met hersenmetastasen (HR 0,67) en Ex19del-mutatie (HR 0,66).3,4 Bij een follow-up van 36 maanden was 60% van de patiënten die behandeld werden met amivantamab + lazertinib in leven versus 51% in de osimertinib-groep. Op 42 maanden was 56% van de patiënten in leven in de combinatiegroep, vergeleken met 44% bij osimertinib. Deze resultaten suggereren dat deze therapie mogelijk de 5-jaarsoverleving aanzienlijk verbetert.3,4
Veiligheidsprofiel
Het veiligheidsprofiel dat uit deze finale analyse van de MARIPOSA-studie volgde was consistent met hetgeen al uit de primaire analyse was gebleken.3,4 De meeste bijwerkingen treden vooral op tijdens de eerste 4 maanden van de behandeling (figuur 2).3,4,12 Bij langere follow-up zijn geen nieuwe veiligheidsproblemen waargenomen, wat erop wijst dat langdurige behandeling haalbaar is.3,4,12
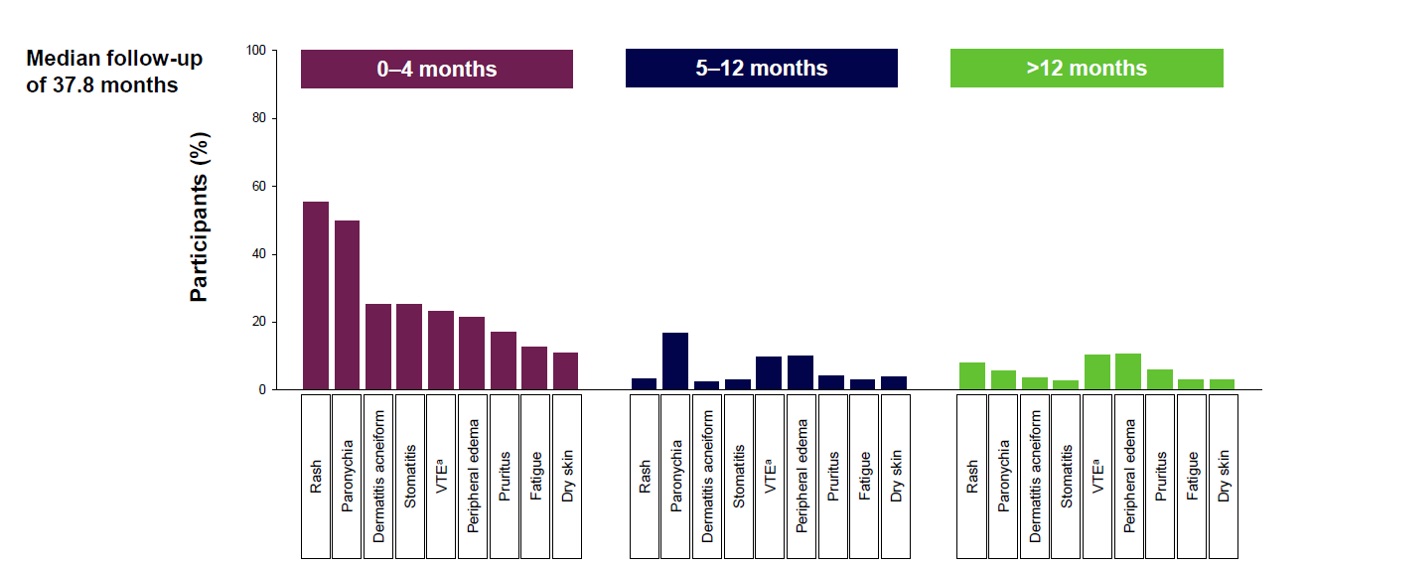
Figuur 2. Bijwerkingen doen zich vooral in de eerste 4 maanden voor3,4,12
De bijwerkingen die zich kunnen voordoen bij de combinatiebehandeling van amivantamab + lazertinib zijn met name dermatologische klachten zoals huiduitslag, paronychia en haaruitval.3,4,12 Deze bijwerkingen kunnen leiden tot dosisverlagingen en onderbreking van de behandeling. Momenteel wordt de profylactische behandeling van dermatologische bijwerkingen onderzocht (eerste data gepresenteerd tijdens ELCC; naar verwachting zullen deze later gepubliceerd worden).
PALOMA-2 en -3: van infuus naar subcutane toediening
PALOMA-2 toont haalbaarheid van subcutaan amivantamab aan
In de PALOMA-2-studie – een fase II-studie die uit 8 cohorten van elk 65 patiënten bestaat – werd onder meer de haalbaarheid onderzocht van het overschakelen van intraveneuze naar subcutane toediening van amivantamab bij patiënten die al intraveneuze therapie kregen. Amivantamab subcutaan – geformuleerd in combinatie met hyaluronidase rHuPH20 – werd handmatig in de buik geïnjecteerd met een dosis van 1.600 mg (of 2.240 mg bij patiënten met een lichaamsgewicht van ≥ 80 kg) op dag 1 en dag 15 van elke cyclus van 28 dagen. Het bleek dat switchen naar subcutane amivantamab monotherapie haalbaar is, waarbij geen toedieningsgerelateerde reacties werden gemeld. Veruit de meeste deelnemers waren tevreden over de subcutane toediening van amivantamab, vonden het gebruiksvriendelijk en gaven de voorkeur aan deze vorm boven de eerdere intraveneuze toediening. Het veiligheidsprofiel van deelnemers die overstapten van amivantamab IV naar amivantamab SC was vergelijkbaar met het eerder waargenomen veiligheidsprofiel van amivantamab SC-monotherapie.5,6,12
PALOMA-3 laat duidelijke voordelen van subcutaan amivantamab zien
De PALOMA-3-studie is een gerandomiseerde internationale fase III-studie die de werkzaamheid, veiligheid en farmacokinetiek onderzoekt van subcutaan versus intraveneus toegediend amivantamab, beide in combinatie met lazertinib, bij patiënten met gemetastaseerd EGFR-gemuteerd NSCLC die eerder progressie hadden doorgemaakt na behandeling met osimertinib en platinagebaseerde chemotherapie.6 418 patiënten werden 1:1 gerandomiseerd naar een van beide behandelarmen. De belangrijkste uitkomstmaten waren de farmacokinetische non-inferioriteit, objectieve respons (ORR), PFS en OS. De resultaten toonden aan dat de subcutane formulering non-inferieur was aan de intraveneuze formulering wat betreft farmacokinetiek. De ORR was vergelijkbaar (30% vs. 33%), terwijl de mediane PFS iets hoger was in de subcutane groep (6,1 vs. 4,3 maanden). Opmerkelijk was dat de algehele overleving significant langer was bij subcutane toediening (HR 0,62; p = 0,02).6 Wat betreft veiligheid waren infusiereacties aanzienlijk lager in de subcutane groep (13% vs. 66%) en de toediening duurde veel korter (4,8 minuten vs. 5 uur bij de eerste dosis).6 Ook werden er minder veneuze trombo-embolische complicaties gerapporteerd in de subcutane groep (9% vs. 14%).6 Patiënten ervoeren de subcutane behandeling als veel gebruiksvriendelijker. De onderzoekers concludeerden dat de werkzaamheid en veiligheid van subcutaan toegediend amivantamab in combinatie met lazertinib van een vergelijkbaar niveau is als intraveneus toegediend amivantamab in combinatie met lazertinib, maar duidelijke voordelen biedt op het gebied van toedieningsgemak, minder veneuze trombo-embolieën en infusie-gerelateerde reacties (IRRs) geeft en resulteert in een verbeterde overleving. Deze bevindingen ondersteunen bredere toepassing van de subcutane toedieningsvorm in de klinische praktijk.6
Synergie MARIPOSA- en PALOMA-studies
De studies samen – MARIPOSA (effectiviteit) en PALOMA-2 en -3 (toedieningsvorm) – laten zien dat de focus op overleving gepaard kan gaan met oog voor kwaliteit van leven en behandelgemak. Waar MARIPOSA de weg opent naar een langere levensverwachting bij EGFR-NSCLC voegt PALOMA daar een patiëntvriendelijk alternatief aan toe met subcutane toediening.3-6,12
Conclusie: een kantelmoment in de behandeling van EGFR-NSCLC
De resultaten gepresenteerd tijdens het ELCC wijzen op een nieuw tijdperk in de behandeling van EGFR-gemuteerde niet-kleincellige longkanker. Niet alleen worden de overlevingskansen aanzienlijk verbeterd, ook zijn er strategieën beschikbaar om de behandeling comfortabeler en effectiever te maken.3-6 De combinatie van amivantamab + lazertinib vertegenwoordigt mogelijk een nieuwe standaard in de eerstelijnsbehandeling. De ontwikkeling van een subcutane formulering van amivantamab maakt de therapie praktischer voor zowel patiënten als zorgverleners. Samen vormen deze studies een krachtig pleidooi voor combinatietherapie met toedieningsgemak; een benadering waarin patiëntuitkomsten én patiëntbeleving centraal staan.3-6,12
Referenties
- Maemondo M, Inoue A, et al. Gefitinib or Chemotherapy for Non–Small-Cell Lung Cancer with Mutated EGFR. N Engl J Med. 2010;362:2380-8.
- Ramalingam SS, Vansteenkiste J, et al; FLAURA Investigators. Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC. N Engl J Med. 2020;382:41-50.
- Yang JC-H, Kim YJ, Lee S-H, et al. Amivantamab Plus Lazertinib vs Osimertinib in First-line EGFR-mutant Advanced NSCLC. ELCC 2025.
- Cho BC, Lu S, Felip E, et al. Amivantamab plus Lazertinib in Previously Untreated EGFR-Mutated Advanced NSCLC. N Engl J Med. 2024;391:1486-98.
- Lim SM, Han J-Y, Zhang J, et al. Subcutaneous after intravenous amivantamab in advanced NSCLC: Initial results from PALOMA-2. ELCC 2025.
- Leigh NB, Akamatsu H, Lim SM, et al. Subcutaneous Versus Intravenous Amivantamab, Both in Combination With Lazertinib, in Refractory Epidermal Growth Factor Receptor–Mutated Non–Small Cell Lung Cancer: Primary Results From the Phase III PALOMA-3 Study. J Clin Oncol. 2024;42:3593-605.
- National Cancer Institute Cancer Stat Facts: Lung and bronchus cancer. Beschikbaar via https://seer.cancer.gov/statfacts/html/lungb.html.
- LUNGevity Foundation. Types of Lung Cancer. Beschikbaar via https://www.lungevity.org/lung-cancer-basics/types-of-lung-cancer.
- Molina JR, Yang P, Cassivi SD, et al. Non-small Cell Lung cancer: epidemiology, risk factors, treatment, and survivorship. Mayo Clin Proc. 2008;83:584-94.
- Richtlijn Niet kleincellig longcarcinoom. https://richtlijnendatabase.nl/richtlijn/niet_kleincellig_longcarcinoom/startpagina_-_niet-kleincellig_longcarcinoom.html
- Morgillo F, Della Corte CM, Fasano M, et al. Mechanisms of resistance to EGFR-targeted drugs: lung cancer. ESMO Open. 2016;1:e000060.
- SmPC Rybrevant https://static.janssen-emea.com/sites/default/files/Benelux/SMPC/BEN-PL-0118.pdf
Deze publicatie werd financieel ondersteund door Janssen-Cilag B.V., een Johnson & Johnson bedrijf (Janssen). Het medical writing werd uitgevoerd door Constance de Koning, wetenschapsjournalist. De standpunten in deze publicatie zijn die van de individuele auteur(s) en weerspiegelen niet noodzakelijk de standpunten van Janssen
Figuur 1. Overall survival in de MARIPOSA-studie3,4
-
Verkorte productinformatie Rybrevant®.
▼ Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden.
Figuur 1. Overall survival in de MARIPOSA-studie3,4Naam van het geneesmiddel: Rybrevant 350 mg concentraat voor oplossing voor infusie. Kwalitatieve en kwantitatieve samenstelling: Eén ml concentraat voor oplossing voor infusie bevat 50 mg amivantamab. Eén injectieflacon van 7 ml bevat 350 mg amivantamab. Amivantamab is een op volledig humaan immunoglobuline G1 (IgG1) gebaseerd bispecifiek antilichaam dat is gericht tegen de epidermalegroeifactor (EGF)-receptoren en tegen de mesenchymale-epitheliale transitie (MET)-receptoren, geproduceerd door een zoogdiercellijn (ovariumcellen van de Chinese hamster, CHO) met behulp van recombinant-DNA-techniek. Farmaceutische vorm: Concentraat voor oplossing voor infusie. De oplossing is kleurloos tot lichtgeel, met een pH van 5,7 en een osmolaliteit van ongeveer 310 mOsm/kg. Therapeutische indicatie: Rybrevant is geindiceerd: • in combinatie met lazertinib voor de eerstelijnsbehandeling van volwassen patiënten met gevorderde niet-kleincellige longkanker (NSCLC) met EGFR Exon 19-deleties of exon 21 L858R-substitutiemutaties; • in combinatie met carboplatine en pemetrexed voor de behandeling van volwassen patiënten met gevorderd NSCLC met EGFR-mutaties bestaande uit exon 19 deleties of exon 21 L858R substituties na falen van eerdere therapie waaronder een EGFR tyrosinekinaseremmer (TKI); • in combinatie met carboplatine en pemetrexed voor de eerstelijnsbehandeling van volwassen patiënten met gevorderd niet-kleincellig longcarcinoom (NSCLC) met activerende insertiemutaties in het exon 20-gen van de EGFR; • als monotherapie voor de behandeling van volwassen patiënten met gevorderd niet-kleincellig longcarcinoom (NSCLC) met activerende insertiemutaties in het exon 20-gen van de epidermalegroeifactorreceptor (EGFR), na falen van op platina gebaseerde therapie. Dosering en wijze van toediening: Zie de volledige SmPC voor meer informatie over de toediening, de behandelschema’s en de geadviseerde premedicatie. Contra-indicaties: Overgevoeligheid voor de werkzame stof(fen) of voor een van de hulpstoffen. Bijzondere waarschuwingen en voorzorgen bij gebruik: • Terugvinden herkomst: Om het terugvinden van de herkomst van biologicals te verbeteren moeten de naam en het batchnummer van het toegediende product goed geregistreerd worden; • Infusiegerelateerde reacties: Vóór de eerste infusie (week 1) moeten antihistaminica, antipyretica en glucocorticoïden worden toegediend om het risico op IRR’s te verkleinen. De infusie dient onderbroken te worden bij het eerste teken van een IRR. Op klinische indicatie moeten aanvullende ondersteunende geneesmiddelen worden toegediend. (zie sectie dosisaanpassingen/infusiegerelateerde reacties in de volledige SmPC); • Huid- en nagelreacties: Als de patiënt een graad ≥ 2-reactie van huid of nagel ontwikkelt, moet ondersteunende zorg worden ingesteld. Zie de volledige SmPC voor meer informatie m.b.t. ondersteunende zorg en dosisverlaging; • Interstitiële longziekte: Behandeling met Rybrevant moet tijdelijk worden gestaakt als interstitiële longziekte (ILD) of op ILD lijkende bijwerkingen (pneumonitis) worden vermoed. Als bevestigd is dat de patiënt ILD of op ILD lijkende bijwerkingen (bijv. pneumonitis) heeft, stop dan definitief met Rybrevant;
Oogaandoeningen:Patiënten die zich presenteren met verergerende symptomen aan de ogen, moeten onmiddellijk naar een oogarts worden verwezen en moeten stoppen met het gebruik van contactlenzen totdat de symptomen zijn beoordeeld. Bijwerkingen: Voor een compleet overzicht, zie de volledige SmPC. Uit de verschillende datasets waarbij amivantamab werd onderzocht als monotherapie (N=380), amivantamab in combinatie met carboplatine en pemetrexed (N=301) en amivantamab in combinatie met lazertinib (N=421) waren de meest frequent (≥20%) waargenomen bijwerkingen van alle graden: rash, IRRs, neutropenie, nageltoxiciteit, hypoalbuminemie, oedeem, vermoeidheid, stomatitis, nausea, trombocytopenie, constipatie, diaree, droge huid, pruritus, verminderde eetlust, hypocalciëmie, hypoalbuminemie, alanineaminotransferase verhoogd, aspartaataminotransferase verhoogd, braken en hypokaliëmie en overige oogaandoeningen. Ernstige bijwerkingen waren onder andere: ILD, IRR, veneuze tromboembolie (VTE), pneumonie, hepatoxiciteit, COVID-19, trombocytopenie, pleurale effusie en rash. De bijwerkingen die het vaakst leidden tot stoppen met de behandeling waren: IRRs, ILD, VTE, nageltoxiciteit, rash. Registratiehouder: Janssen-Cilag NV, Turnhoutseweg 30, B-2340 Beerse, België. ATC code: Farmacotherapeutische categorie: Monoklonale antilichamen en antilichaam geneesmiddelconjugaten. Uitgebreide productinformatie: Voor volledige SmPC: https://innovativemedicine.jnj.com/netherlands/products. Afleveringswijze: Geneesmiddel op medisch voorschrift. Datum: 19/12/2024.Telefoon: 0800 242 42 42 E-mail: info_nl@its.jnj.com Internet: www.janssen.com/nederland
CP-519357