Van 13 t/m 16 maart vond in Londen de 41ste editie plaats van het jaarlijkse EAU Congres. Toonaangevende experts en jonge urologen kwamen bijeen om nieuw onderzoek te delen, innovaties te verkennen en van elkaar te leren. Hier volgt een selectie van de highlights. Lees het volledige dossier op mednet.nl/oncologie.
Enfortumab vedotin + pembrolizumab bij MIBC: KEYNOTE-B15
Enfortumab vedotin (EV) plus pembrolizumab is de eerste combinatie van een antilichaam-geneesmiddelconjugaat (ADC) met een immuuncheckpointremmer met een gunstiger eventvrije overleving (EFS), algehele overleving (OS) en pathologisch complete respons (pCR) dan neoadjuvante chemotherapie op basis van cisplatine, bij spierinvasieve blaaskanker (MIBC).
KEYNOTE-B15 was een fase III-studie bij MIBC-patiënten die kwalificeerden voor cisplatine en een radicale cystectomie, en bekkenlymfadenectomie ondergingen. De 808 deelnemers werden gerandomiseerd naar ofwel neoadjuvant EV plus pembrolizumab gevolgd door chirurgie en adjuvant EV plus pembrolizumab (n = 405); ofwel standaard neoadjuvant cisplatine-gemcitabine gevolgd door chirurgie en observatie (n = 403). De gemiddelde follow-up na randomisatie was 33,6 maanden. Het primaire eindpunt was de EFS.
De 3 belangrijkste eindpunten (soms niet bereikt: NR) vielen alle 3 significant positiever uit in de experimentele arm:
- Mediane EFS in maanden: NR (NR-NR) versus 48,5 (43,3-NR); hazard ratio 0,53 (95%-BI 0,41-0,70; eenzijdige p < 0,0001). Percentage EFS na 24 maanden: 79,4% versus 66,2%.
- Mediane totale overleving (OS) in maanden: NR (NR-NR) versus NR (NR-NR); hazard ratio 0,65 (95%-BI 0,48-0,89; eenzijdige p = 0,0029). Percentage OS na 24 maanden: 86,9% versus 81,3%.
- Pathologisch complete respons (pCR): 226 patiënten (55,8%; 95%-BI 50,8-60,7) versus 131 (32,5%; 95%-BI 28,0-37,3). Geschat verschil: 23,4% (95%-BI 16,7-29,8; eenzijdige p < 0,0001). Deze verbetering vertaalde zich in een overlevingsvoordeel.
De chirurgische uitkomsten en bijwerkingen tijdens de chirurgische fase waren vergelijkbaar tussen de armen. Een vergelijkbaar percentage deelnemers onderging een cystectomie en had daarna negatieve snijranden. Het veiligheidsprofiel van neoadjuvant en adjuvant EV plus pembrolizumab was consistent met eerdere ervaringen. Volgens de auteurs is het hiermee een nieuwe behandeloptie bij MIBC, ongeacht of patiënten in aanmerking komen voor cisplatine.
Bron:
Galsky M, et al. EAU26, GC26-009.
Screenen op prostaatkanker in de populatie: resultaten na 30 jaar
Van 20.000 oudere Zweedse mannen heeft de helft zich de afgelopen 30 jaar in studieverband laten screenen op prostaatkanker, de andere helft niet. Het resultaat was een aanzienlijke en langdurige verlaging van de mortaliteit door prostaatkanker. Er waren ook veel (permanent) vals-positieve diagnoses.
De resultaten na 30 jaar van de Gothenburg 1-studie werden gepresenteerd door dr. Jonas Hugosson uit Göteborg. In 1994 werden 20.000 mannen van 50-64 jaar 1:1 gerandomiseerd naar de screeningsgroep (SG) of controlegroep (CG), vertelde hij. Mannen in de SG werden tot hun 70ste elke 2 jaar uitgenodigd om het prostaatspecifiek antigeen (PSA) te bepalen. Bij een PSA ≥ 3 ng/ml werd doorverwezen voor biopten. In de controlegroep werd alleen opportunistisch gescreend.
Dr. Hugosson vertelde dat van de 10.000 mannen die daartoe waren uitgenodigd, 7.653 (77%) zich minstens 1 keer lieten screenen. Daar kwam bij 2.673 mannen minstens 1 keer een verhoogde PSA-waarde uit; 95% accepteerde een systematische biopsie. De tumoren die met screening werden gevonden, waren voor 80% International Society of Urological Pathology (ISUP) stadium 1; bij 46% werd (aanvankelijk) volstaan met actieve monitoring.
Na 30 jaar follow-up was bij 1.711 mannen in de SG en bij 1.373 in de CG de diagnose prostaatkanker gesteld. Het relatieve risico was na 15, 20, 25 en 30 jaar follow-up respectievelijk 1,60; 1,54; 1,35 en 1,30. Het absolute verschil in mortaliteit door prostaatkanker werd tussen jaar 15 en 30 elke 5 jaar hoger (zie tabel 1).
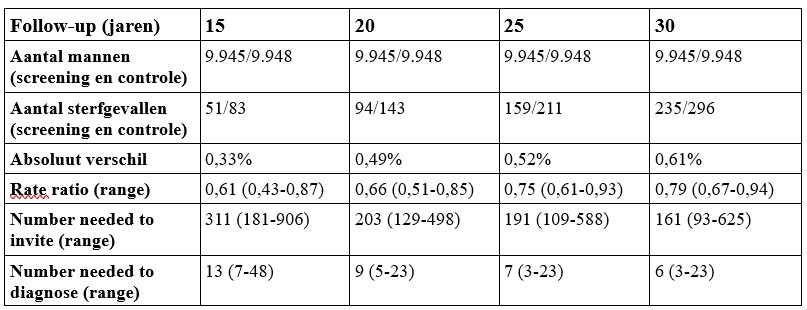
Tabel 1. Resultaten rond mortaliteit van the Gothenburg 1-studie.
Dr. Hugosson concludeerde dat screening op PSA en het afnemen van biopten de mortaliteit door prostaatkanker aanzienlijk en langdurig verlaagt. “The number needed to invite” om 1 overlijden te voorkomen, was 161. Een zo laag aantal is bij kankerscreening nooit eerder gezien. “The number needed to diagnose” is 6; vergelijkbaar met screening op borstkanker bij vrouwen, zij het minder snel bereikt. Dr. Hugosson zag ook een nadeel: het hoge percentage overdiagnoses. “Screeningsprogramma’s moeten zich daarom focussen op risicostratificatie en het selectiever uitvoeren van biopsies, zonder het uitzicht op genezing te verliezen.”
Bron:
Hugosson J, et al. EAU26, GC26-002.
Tranexaminezuur verlaagt bloedingsrisico bij urologische ingrepen
De resultaten van de internationale gerandomiseerde en placebogecontroleerde POISE-3-trial ondersteunen profylactisch gebruik van tranexaminezuur (TXA) bij urologische chirurgie. TXA vermindert het absolute risico op een ernstige bloeding met 3,4%, wat overeenkomt met een relatieve reductie van 37%. Er was geen duidelijk signaal van een toename in het tromboserisico.
Prof. dr. Kari Tikkinen (Helsinki, Finland) presenteerde de resultaten van de zogeheten POISE-3-trial. De 1.124 deelnemers waren 45 jaar of ouder en ondergingen chirurgie met een verhoogd bloedings- en cardiovasculair risico. Ze werden 1:1 gerandomiseerd naar TXA (1 g intraveneuze bolus aan het begin en einde van de operatie) of placebo. Er waren samengestelde primaire uitkomstmaten voor zowel effectiviteit (bloeding) als veiligheid (trombose).
De 1.124 patiënten waren gemiddeld 70 jaar oud, waarvan 880 (78,3%) mannen, 658 (58,5%) hadden actieve kanker en 284 (25,2%) gebruikten antitrombotica binnen 24 uur voor de operatie. De ingreep was laparoscopisch/robotgeassisteerd bij 489, open bij 360, transurethraal bij 244 en percutaan bij 31. De meest uitgevoerde procedures waren een robotgeassisteerde radicale prostatectomie (n = 156) en een TURP (n = 138).
Bloeding trad op bij 45 (8,1%) patiënten in de TXA-groep en bij 62 (10,9%) in de placebogroep (HR 0,73; 95%-BI 0,50-1,07; p = 0,11). Ernstige bloedingen traden op bij respectievelijk 34 (6,1%) en 54 (9,5%) patiënten (RR 0,63; 95%-BI 0,41-0,97; p = 0,03). Trombose trad op bij 67 (12,1%) patiënten in de TXA-groep en bij 62 (10,9%) in de placebogroep (HR 1,12; 95%-BI 0,79-1,58; p = 0,52). “Ik wil me hard maken voor meer gebruik van TXA”, besloot prof. dr. Tikkinen. “Het is goedkoop, eenvoudig toe te dienen en helpt bloedingen en transfusies verminderen.”
Bron:
Tikkinen KAO, et al. EAU26, GC26-001.
Pembrolizumab + belzutifan verhoogt ziektevrije overleving bij ccRCC
LITESPARK-022 is de eerste positieve fase III-trial van adjuvant pembrolizumab in combinatie met belzutifan bij niercelcarcinoom (RCC). Het was geassocieerd met een significant betere ziektevrije overleving (DFS) bij heldercellig RCC (ccRCC), ongeacht de aanwezigheid van sarcomatoïde kenmerken.1
Adjuvant pembrolizumab verbeterde de DFS en totale overleving (OS) in de placebogecontroleerde KEYNOTE-564-trial.2 In de LITESPARK-022-trial is gekeken of dit effect verder verhoogd kan worden door de hypoxie-induceerbare factor 2α (HIF-2α)-remmer belzutifan toe te voegen bij ccRCC-patiënten met een verhoogde recidiefkans na nefrectomie. Prof. dr. Thomas Powles (Londen, Groot-Brittannië) presenteerde de resultaten.1 Hij zei dat de studiepopulatie sterke gelijkenis vertoonde met die van de KEYNOTE-564. De 1.841 deelnemers kregen pembrolizumab 400 mg om de 6 weken (≤ 9 doses) plus eenmaal daags belzutifan 120 mg of placebo. Het primaire eindpunt was de DFS. Belzutifan resulteerde in een statistisch significante en klinisch belangwekkende verbetering van de DFS (HR 0,72; 95%-BI 0,59-0,87; p = 0,0003). Het veiligheidsprofiel van de combinatie was consistent met de verwachtingen voor elk afzonderlijk geneesmiddel.3
Prof. dr. Powles presenteerde in meer detail de uitkomsten van tussentijdse exploratieve analyses van de effectiviteit, na een mediane follow-up van 28,4 maanden. Dit waren de belangrijkste resultaten (in de intention-to-treat-populatie):
- Het gunstige effect van de combinatie pembrolizumab plus belzutifan was onafhankelijk van sarcomatoïde groei. Bij aanwezigheid daarvan was de HR voor events 0,55 (95%-BI 0,34-0,88); bij afwezigheid 0,72 (95%-BI 0,58-0,90).
- Verkennende analyses van de metastasevrije overleving (DMFS) en PFS na 2 weken gaven een gunstiger beeld in de belzutifan-groep: HR 0,71 (95%-BI 0,59-0,87).
- Van de deelnemers met een recidief ontving het merendeel (> 80%) vervolgbehandeling. Meestal (> 60%) was dat systemische therapie.
- Tijd tot progressie op een behandeling in de volgende lijn of overlijden (PFS2: een indicator voor de toekomstige OS) was in de belzutifan-groep gunstiger: HR 0,68 (95%-BI 0,48-0,94).
Prof. dr. Powles concludeerde: “De resultaten ondersteunen standaardgebruik van adjuvant pembrolizumab plus belzutifan in deze setting.”
Bronnen:
- Powles T, et al. EAU26, GC26-007.
- Choueiri TK, et al. N Engl J Med. 2021;385:683-94.
- Choueiri TK, et al. J Clin Oncol. 2026;44:LBA418.
Blauwlicht-TUR-BT en optimale MMC verlaagt recidiefkans NMIBC
Transurethrale resectie van een blaastumor (TUR-BT) met blauw licht, gevolgd door adjuvante geoptimaliseerde chemotherapie met mitomycine-C (MMC) is een relatief effectieve manier om de recidiefkans te verlagen bij hoogrisicopatiënten met laaggradig papillair urotheelcarcinoom (pTa). Dit blijkt uit resultaten van de FinnBladder-9-studie.
Patiënten met laaggradig papillair niet-spierinvasief blaascarcinoom (pTa) met een hoog risico op recidief werden gerandomiseerd naar 1 van 4 groepen: A) TUR-BT met wit licht zonder adjuvante therapie; B) TUR-BT met blauw licht zonder adjuvante therapie; C) TUR-BT met wit licht en 6-wekelijkse geoptimaliseerde MMC; D) TUR-BT met blauw licht en 6-wekelijkse geoptimaliseerde MMC. De randomisatie vond plaats vóór de TUR-BT en werd gestratificeerd op basis van ziekenhuis en recidiefgeschiedenis. Het primaire eindpunt was recidief.
In 10 jaar (2012-2022) werden 269 patiënten gerandomiseerd. De mediane leeftijd was 72 jaar; 56% had primaire tumoren, 43% multipele tumoren en 15% tumoren van ≥ 3 cm. De mediane follow-up bedroeg 5,2 jaar. Het recidiefpercentage in de studie als geheel was 35%. Groep D had significant minder recidieven dan groep A: HR 0,43 (95%-BI 0,22-0,81, p = 0,010). Er werden geen significante verschillen in recidiefkans en totale overleving tussen de andere armen vastgesteld. Het risico op progressie was erg laag (1,6%), zonder verschillen tussen de studiearmen.
Bron:
Boström PJ, et al. EAU26, LB009.
FDG-PET/CT waardevol bij stadiëring subtype invasieve blaaskanker
FDG-PET/CT (18F-fluorodeoxyglucose positron emissie tomografie/computertomografie) kan, naast conventioneel urotheelcelcarcinoom (UC), ook bij blaaskanker met histologische subtypen (HS’en) de primaire tumor visualiseren en aanvullende informatie geven over de stadiëring van de tumor. Dit blijkt uit Amsterdams onderzoek.
Het stadium van invasieve blaaskanker (IBC) wordt doorgaans bepaald met een CT-urografie of MRI. Als hieraan PET-CT wordt toegevoegd, wijzigt dat de stadiëring bij ongeveer een kwart van de patiënten, vertelde Renee Lijnen van het Amsterdam UMC. Bij ongeveer 1 op de 5 patiënten verandert dan ook de behandeling. Dit betreft echter conventioneel UC. Tot 25% van de blaaskankers kent hiervan afwijkende HS’en, geassocieerd met minder gunstige uitkomsten.
De optimale manier om HS’en van invasieve blaaskanker te stadiëren is nog onbekend. De studie van Lijnen en collega’s evalueert de diagnostische prestaties en klinische waarde van FDG-PET/CT bij de stadiëring van IBC met zeldzame HS-cellen.
Ze includeerden 112 patiënten met histologisch bevestigde IBC met ≥ 75% HS-cellen. De mediane leeftijd was 67 jaar; 95% had spierinvasieve ziekte. De HS’en betroffen neuro-endocriene tumoren (40%), plaveiselcelcarcinomen (34%), adenocarcinomen (11%), sarcomatoïde carcinomen (11%) en overige (4%). Van de HS’en was 82-95% zichtbaar op FDG-PET/CT. Slechts 4% was FDG-negatief. FDG-PET/CT leidde tot een wijziging – meestal verhoging – van de klinische stadiëring bij 20% van de patiënten.
Deze resultaten suggereren dat de meeste HS’en van IBC voldoende metabolische activiteit behouden voor FDG-PET-beeldvorming, dat daarmee aanvullend kan worden ingezet om zeldzame HS’en te stadiëren.
Bron:
Lijnen R, et al. EAU26, A0872.